 Pengobatan penyakit di masa depan tak sebatas mengatasi gejala dan manifestasi. Pengobatan ditujukan langsung ke ”sumber masalah” di tingkat gen, terutama untuk penyakit akibat kelainan genetik, seperti talasemia. Penelitian di tingkat gen memberikan harapan baru bagi penderita.
Pengobatan penyakit di masa depan tak sebatas mengatasi gejala dan manifestasi. Pengobatan ditujukan langsung ke ”sumber masalah” di tingkat gen, terutama untuk penyakit akibat kelainan genetik, seperti talasemia. Penelitian di tingkat gen memberikan harapan baru bagi penderita.Ahli dari Molecular Genetics and Gene Regulation School of Biotechnology and Biomolecular Sciences, University of New South Wales, Sydney, Australia, Merlin Crossley dan rekan-rekan, memanfaatkan modulasi gen dan pengaturan ekspresi gen guna mengatasi talasemia. Crossley memaparkan dalam seminar ”Modulating Gene Expression in Human Genetic Disease” di Kedutaan Besar Australia, Mei.
”Manusia pada dasarnya merupakan mutasi. Seorang anak membawa paduan gen dari bapak dan ibunya,” kata Crossley. Ekspresi gen dalam tubuh manusia dapat diregulasi, yakni dipadamkan atau dinyalakan.
Talasemia, misalnya, merupakan mutasi yang tak lepas dari perlawanan tubuh terhadap malaria. ”Penyakit talasemia banyak terdapat di daerah berjangkitnya malaria atau pernah menjadi daerah endemik malaria, seperti di daerah tropis, Eropa tenggara, mediterania, dan Timur Tengah,” ujarnya.
Parasit malaria berkembang di sel darah merah sehat. Perubahan kecil di satu gen globin—setiap orang mempunyai dua gen globin, yakni satu dari ibu dan satu dari ayah—dapat melemahkan sel darah merah sehingga parasit malaria tidak bisa tinggal. ”Mutasi ini tidak buruk bagi mereka yang tinggal di daerah malaria karena menjadi perlindungan diri. Mutasi hanya pada satu globin tidak menimbulkan gejala sakit, orang terkait tetap sehat, tidak terkena malaria,” kata Crossley.
Masalah timbul ketika dua orang yang mengalami mutasi di salah satu gen globinnya menikah. Anak yang dilahirkan berpeluang lahir dengan mutasi ganda karena mendapatkan salinan dari gen globin ayah ibunya sehingga mengalami talasemia berat.
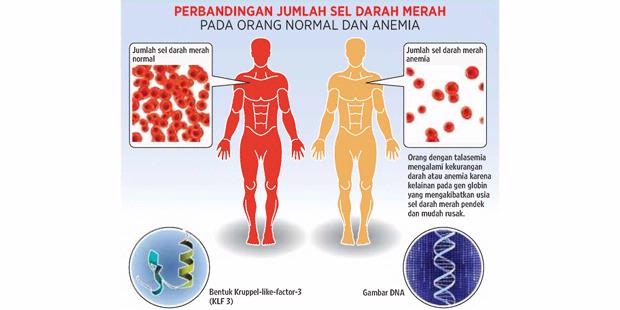
Kelainan gen globin pada talasemia berat mengakibatkan rantai globin berkurang. Rantai yang tak utuh membuat keping darah mudah pecah (sel darah merah berumur pendek) dan melepaskan zat besi yang merupakan unsur pengikat hemoglobin. Akibatnya, penderita kekurangan darah dan terancam jiwanya. Di Indonesia, usia harapan hidup orang dengan talasemia sekitar 30 tahun jika didukung transfusi darah rutin dan obat penguras zat besi (khelasi).
Ubah ekspresi gen
Modulasi gen adalah praktik mengubah ekspresi gen. Dalam kasus talasemia, pengaktifan kembali ekspresi gen globin janin menawarkan obat potensial untuk talasemia.
Menurut Crossley, hal itu didasarkan pada kenyataan saat dalam kandungan, bayi dengan talasemia tumbuh normal karena mempunyai gen globin janin. Gen itu mampu mengikat oksigen untuk memastikan pasokan oksigen memadai dari ibu.
Begitu bayi lahir, kata Crossley, gen globin dewasa mulai aktif dan gen globin janin padam. Pada orang dengan talasemia berat, gen globin dewasa tidak bekerja baik lantaran terjadi mutasi. ”Namun, ada segelintir orang yang gen globin janinnya menyala sepanjang hidup mereka. Mereka yang talasemia dapat hidup normal,” katanya.
Berangkat dari perkecualian itu, penelitian dilakukan di pelbagai pusat riset di dunia dengan harapan jika gen globin janin pada orang dengan talasemia dapat dinyalakan kembali, penyakit itu bisa disembuhkan.
Crossley mengatakan, terdapat protein pengikat DNA (DNA binding protein) yang berperan memadamkan gen globin janin. Protein ini termasuk faktor yang mengatur proses transkripsi dan pembelahan molekul DNA.
Para peneliti, termasuk Crossley, berupaya mendapatkan protein yang berperan membuat gen globin janin padam. Crossley memfokuskan penelitian pada kelompok Kruppel-like factor (KLF) yang terdiri atas 17 protein. KLF sebagai faktor transkripsi merupakan regulator kunci dari ekspresi gen globin dalam pembentukan sel darah.
Crossley dan rekan-rekan menyelidiki deretan peranti sinyal dan jaringan protein KLF dalam ekspresi gen globin untuk mengaktifkan kembali gen globin janin. Mereka menginvestigasi dua protein yang dicurigai berperan dalam meredam gen globin janin, yakni KLF 3 dan KLF 8. KLF 3 adalah penekan transkripsi.
Para peneliti merekayasa genetik sel induk embrionik tikus percobaan sehingga dihasilkan tikus tanpa KLF 3. Setelah itu mengamati ekspresi gen. Ternyata menghilangkan KLF 3 tidak mengubah ekspresi gen. ”Setidaknya perlu dua protein yang dihambat,” kata Crossley.
Kemudian, peneliti mengamati ekspresi gen yang dimutasi pada KLF 3 dan KLF 8. Hasilnya, sejumlah gen meningkat ekspresinya dan ada yang terkait dengan gen globin janin.
Hasil penelitian itu masih sangat awal. ”Belum ada obat untuk memadamkan KLF 3 dan KLF 8. Kami tidak bisa ’memadamkan’ KLF 3 dan KLF 8 pada manusia seperti pada tikus. Itu tidak etis,” kata Crossley.
Tim menginvestigasi cara kerja tubuh dalam mengaktifkan KLF 3 dan KLF 8, lantas mengembangkan strategi untuk menghambat pembentukan kedua protein dalam tubuh. ”Ini merupakan perjalanan panjang. Hasilnya baru akan dirasakan di masa depan,” katanya.
KLF 3 dan KLF 8 dapat diregulasi antara lain melalui proses peredaman ekspresi gen dan protein dengan mekanisme RNA interference (RNAi). Asam ribonukleat (RNA) merupakan substansi genetik yang menjadi perantara dalam penyandian protein dari gen dalam DNA.
Crossley mengatakan, pihaknya menginvestigasi kinase dalam kelompok homeodomain-interacting protein kinase yang tampaknya meregulasi KLF 3 dan KLF 8.
Enzim inhibitor yang khusus menghalangi dari protein kinase atau koenzim NADH dianalogikan dapat melepaskan gen globin janin yang tertekan atau teredam. Tim lain meneliti penekan lain dari gen globin janin. Ada pula tim yang mencari gen yang mendukung gen globin janin untuk ”menyala” kembali.
Tidak hanya talasemia
Crossley mengatakan, penelitian modulasi gen tidak hanya pada talasemia, tetapi juga pada hemofilia. Pada orang dengan hemofilia, terjadi mutasi yang meredam gen sehingga faktor pembeku IX tereliminasi dan pembekuan darah sulit terjadi. Namun, terdapat sebuah kasus di mana orang dengan hemofilia membaik setelah memasuki pubertas. Terjadi mutasi yang mencegah protein pengikat DNA untuk berikatan.
”Ternyata, testosteron memegang peranan. Testosteron dapat merangsang ekspresi dari faktor pembekuan darah IX,” ujarnya.
Namun, terlalu berbahaya menggunakan hormon testosteron untuk mengatasi hemofilia karena dapat mengganggu fungsi tubuh lain. Selain itu, ada juga kasus pasien yang tidak sembuh setelah pubertas karena ada mutasi gen lain.
Penyakit lain, seperti obesitas, juga menjadi wilayah penelitian modulasi gen. Tikus yang KLF 3-nya dipadamkan menjadi kurus dengan kadar lemak tubuh yang rendah.
Oleh : Indira Permanasari
kompas.com




Tidak ada komentar:
Posting Komentar